23 avril 2020 - La biothérapie tocilizumab ou le nouveau défi du traitement de la Covid-19
Correspondance : Daniel Letonturier
Service de médecine gériatrique aiguë (unité Covid), hôpital gériatrique de l’Isle-Adam Parmain, France
Mots clés : coronavirus, Covid-19, tocilizumab, choc cytokinique, syndrome de libération des cytokines, interleukine 6, inhibiteur du récepteur à l’interleukine 6
⇐ Retour au dossier "Actualités COVID-19"
De nombreuses cytokines ont été ientifiées dans la pathogénicité de la maladie Covid-19, et plusieurs études ont fait état du bénéfice thérapeutique de certains biosimilaires tels que les anti-facteur de nécrose tumorale (TNF)-α et les antagonistes d’interleukines (IL). Le tocilizumab est un anticorps monoclonal recombinant humanisé dirigé contre le récepteur de l’IL-6, qui pourrait être efficace dans les cas d’infection virale. Plusieurs cas-patients de rémission précoce et prolongée de l’infection sous ces traitements sont rapportés.
Comment de tels produits peuvent-ils agir ? Il faut, pour le comprendre, envisager la pathologie Covid-19 non comme une « simple » infection, mais comme une maladie évolutive à la fois virale, inflammatoire, immunologique et vasculaire – donc systémique – aiguë. L’intérêt thérapeutique de ces biosimilaires procède de ce qu’il agit sur le processus d’inflammation aiguë qui survient dans la Covid-19 et est susceptible d’induire une défaillance respiratoire d’origine pulmonaire ou multiviscérale. L’existence d’un syndrome de libération des cytokines (CRS), et son rôle délétère, dans les formes les plus graves de la maladie, sont désormais bien établis [1]. Souvant appelé choc ou décharge cytokinique, il correspond à des taux élevés de cytokines – notamment les IL-6, 2, 7, 10 et 12, les facteurs stimulant les colonies de granulocytes (G-CSF) et de macrophages (GM-CSF), le TNF-α et l’interféron [IFN] γ – produites par une prolifération majeure de cellules immunitaires activées (lymphocytes T, monocytes, macrophages). On parle même de lymphohistiocytose hémaphagocytaire secondaire (sHLH), à l’origine d’une libération cytokinique fulminante amenant l’organisme humain à décompenser vers une défaillance multiorganique et vers la mort. Ce syndrome survient dans 3,7 à 4,3 % des cas de sepsis bactérien sévère ; des infections virales peuvent également en être cause. Les manifestations en sont une fièvre incessante, des cytopénies, une hyperferritinémie et une insuffisance respiratoire aiguë – jusqu’à un syndrome de détresse respiratoire aiguë chez environ 50 % des patients. Une correspondance adressée au Lancet [2] a d’ailleurs relevé que, chez les 150 patients de Wuhan atteints de Covid-19 suivis par une étude chinoise, des taux très élevés d’hyperferritinémie et d’IL-6 constituaient des prédicteurs de morbimortalité, suggérant que la mortalité imputable à la Covid-19 serait directement corrélée à cette hyperinflammation d’origine immunologique (et non virologique), laquelle n’avait pas été contrôlée précocement.
La mise au point de Chi Zhang et al. sur le syndrome de libération cytokinique [3]
Le récepteur de l’IL-6 (IL-6R) possède deux formes : l’une fixée à la membrane des cellules, l’autre soluble. La liaison de l’IL-6 à son récepteur soluble entraîne la formation d’un complexe, qui peut à son tour se fixer sur la glycoprotéine membranaire gp130, induisant la transduction d’un signal intracellulaire, lui-même responsable du déclenchement de la pro-inflammation. Une stratégie thérapeutique consisterait alors à bloquer l’action du complexe IL-6/gp130. L’IL-6 est produite par l’ensemble des cellules du système immunitaire (lymphocytes B et T, macrophages, monocytes) en réaction à la présence d’un agent pathogène. La surexpression d’IL-6 initie la cascade inflammatoire qui assure la défense de l’hôte face à l’intrusion de corps étrangers ou d’agents infectieux. L’il-6 exerce plusieurs effets, favorables ou funestes (figure 1) :
– induire la prolifération et la différenciation des cellules B, puis leur production d’anticorps en réponse à un antigène,
– activer les cellules T et déclencher leur activité cytotoxique,
– activer la synthèse des protéines de la phase aiguë d’inflammation, telles que la protéine C réactive (CRP), par les hépatocytes,
– stimuler l’hématopoïèse dans la moelle osseuse, notamment la différenciation des cellules souches en colonies cellulaires sanguines matures,
– participer à la malignité de processus tumoraux et au développement d’éventuelles pathologies auto-immunes,
– participer au développement des maladies cardiovasculaires ischémiques en rapport avec l’artériosclérose et l’hypertension.
Dans l’emballement du système immunitaire lié à un CRS, le mécanisme de déclenchement pathogénique serait le suivant :
– le virus Sars-Cov-2 infecte les cellules épithéliales alvéolaires, principalement les pneumocytes de type 2 du tissu pulmonaire, grâce à son ancrage sur un récepteur (figure 2),
– la destruction des cellules pulmonaires où ont proliféré les coronavirus par réplication de leur ARN, et l’augmentation de leur perméabilité cellulaire, aboutit au relargage de virus,
– il se produit un réveil du système immunitaire inné par lequel les acteurs de la défense de l’hôte (macrophages, lymphocytes, monocytes, granulocytes) se mettent non seulement à capturer le virus mais aussi à produire une décharge de chimiokines et de cytokines dont l’IL-6.
Une réaction immunitaire adaptée est également activée par les cellules présentatrices d’antigènes ou de particules virales, principalement les cellules dendritiques. Les lymphocytes T et B sont ainsi à même d’assurer la sécrétion des cytokines de l’inflammation, directement ou indirectement, par le biais de médiateurs ou de signaux. Le mécanisme du choc cytokinique résulterait ainsi d’une libération excessive et non régulée de cytokines. Ses manifestations cliniques – dyspnée puis de détresse respiratoire aiguë – résulteraient d’un envahissement alvéolaire massif par les exsudats inflammatoires et d’effusions sanguines érythrocytaires (œdème aigu pulmonaire [OAP] lésionnel).
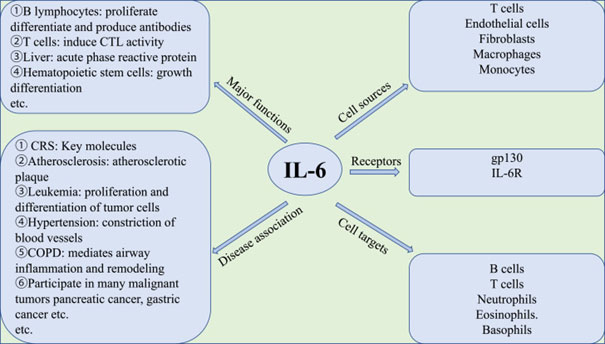
Figure 1
Le rôle physiologique central de l’interleukine 6 dans le métabolisme humain, d’après [3].
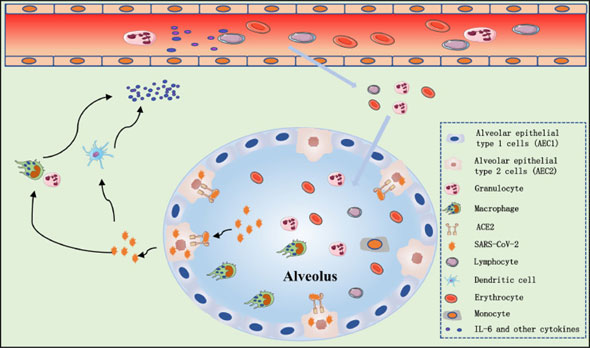
Figure 2
Le mécanisme pathogénique du syndrome de libération cytokinique dans les cas sévères d’infection Covid-19, d’après [3].
À propos de l’analyse de deux cas-patients traités par le tolicizumab
La première observation concerne un patient chinois, originaire de Wuhan, âgé de 60 ans. Il est atteint d’un myélome multiple à immunoglobine [Ig] Aλ, stable et traité au long cours par le thalidomide. Touché par une infection Covid-19 sévère, il a reçu un traitement par tocilizumab, qui s’est révélé être un succès [4]. Il s’est d’abord plaint d’une oppression thoracique isolée, sans fièvre ni toux. Il a été d’emblée hospitalisé devant l’atteinte lésionnelle pulmonaire, dont témoignait des opacités multiples, à aspect de verre dépoli, au scanner thoracique. Le traitement initial a été une antibiothérapie (moxifloxacine) par voie intraveineuse (IV) (400 mg/j sur trois jours), relayée par l’antiviral umifénovir per os (200 mg ´3 par jour) en raison de la positivité du test PCR pour le SARS-CoV2 sur prélèvement pharyngé. L’état respiratoire s’est dégradé à J15, malgré l’oxygénothérapie (3 L/24 h) et une corticothérapie IV à base de méthylprednisolone 40 mg/j (désaturation < 93 %, essoufflement, amplification de l’oppression thoracique) définissant un stade sévère de la maladie Covid-19 – diagnostic rendorcé par la biologie, qui montrait une lymphopénie et un taux sérique isolé très élevé d’IL-6 (plus de 50 fois la normale), sans anomalie des autres cytokines mesurées (IL-2, 4 et 10, TNFα) ni du rapport lymphocytaire T CD4/CD8. L’administration du tolicizumab est instaurée à J24 par voie IV à la posologie de 8 mg/kg. En trois jours, à J27, le patient est soulagé de ses symptômes respiratoires, dont l’oppression, et montre une normalisation du taux d’IL-6. Le patient sera finalement déclaré guéri de la Covid-19, devant la régression très nette des lésions pulmonaires sur scanner thoracique de contrôle ; il sort d’hospitalisation à J42. Dans cette observation, le tolicizumab, en inhibant le récepteur de l’IL-6, a permis de sauver le patient d’une mort certaine, ainsi que de lui éviter une ventilation mécanique invasive. La tolérance du produit a été satisfaisante.
La deuxième observation intéresse un patient âgé de 42 ans suivi pour un carcinome rénal à cellules claires de type sarcome métastatique hospitalisé dans un contexte de douleurs osseuses, fièvre et décision d’une première cure de chimiothérapie [5]. Malgré l’antibiothérapie par ceftriaxone, à J6, la fièvre réapparaît avec une toux en rapport avec la positivité du test PCR pharyngé pour le SARS-Cov2 et la visualisation de lésions pulmonaires bilatérales irrégulières avec images en verre dépoli au scanner thoracique. Le traitement antiviral combinant lopinavir 400 mg + ritonavir 100 mg per os est entrepris dès J7, pour cinq jours. Face à une insuffisance respiratoire aiguë apparue à J8, le patient reçoit une cure de 24 h du produit tocilizumab 8 mg/kg en deux fois. Il s’ensuit rapidement une amélioration clinique nette, le patient devenant afébrile et progressivement eupnéique avec à J12, là encore, une régression des infiltrats pulmonaires et une normalisation de la CRP en quatre jours. Le profil de tolérance est sans particularités.
Pour la pratique dans le contexte actuel de la maladie Covid-19
Ces deux observations cliniques récentes, dans le contexte de la pandémie Covid-19, suggèrent que le tocilizumab s’oppose à la libération cytokinique massive liée à la dérégulation du système immunitaire. Il s’agit en effet d’un anticorps monoclonal ciblant électivement le récepteur de l’IL-6 soluble et inhibant ainsi la transduction d’un signal cellulaire et, partant, toute une cascade de réactions immunitaires défavorables. Ces deux observations ont cependant des limites. Il s’agit, dans les deux cas, de patients immunodéprimés puisque atteints de cancers potentiellement évolutifs, traités de surcroît par des thérapeutiques affectant la fonction immunitaire telles que des cures de corticothérapie. Il est donc, en l’état, difficile d’extrapoler l’efficacité thérapeutique du tocilizumab à d’autres populations, en particulier non cancéreuses. Il avait de surcroît été fait préalablement usage, dans les deux cas-patient, de produits antiviraux (umifénovir pour l’un, lopinavir-ritonavir pour l’autre), qui semblent avoir été inefficaces, et n’ont du moins pas empêché la survenue d’une insuffisance respiratoire aiguë. Cette inefficacité doit encore être démontrée selon l’evidence-based-medecine.
Des essais cliniques randomisés en double aveugle et contrôlés contre placebo sont donc encore nécessaires pour établir, d’une part, si le tocilizumab est réellement efficace chez les patients infectés Covid-19 en situation d’insuffisance respiratoire aiguë, et, d’autre part, le stade clinique de la maladie auquel le produit devrait être utilisé. Le profil de tolérance du tocilizumab et ses éventuelles interactions médicamenteuses avec les antiviraux seront également à établir dans les essais cliniques. Dans ses indications en rhumatologie, il est admis que les principaux effets indésirables [3-5] sont l’anaphylaxie et des réactions allergiques sévères, une leucopénie transitoire, un risque infectieux bactérien, viral et fongique logiquement augmenté, une augmentation du taux des enzymes hépatiques, voire une insuffisance hépatocellulaire, une perforation intestinale, une tuberculose, une réactivation d’hépatite B et une ostéonécrose de la mâchoire [6].
Une étude intéressante, prépubliée sur un site médical chinois, rapporte une série de 21 cas graves de sujets infectés ayant bénéficié d’une cure de tocilizumab dans la période du 5 au 14 février 2020 au sein de deux hôpitaux de la province d’Anhui en Chine orientale [7]. La moyenne d’âge est de 56,8 ans (± 16,5 ; 25-88 ans) ; 85,7 % sont des hommes et 14,3 % des femmes, le plus souvent initialement exposés en zone épidémique de Wuhan ou ayant été en contact étroit avec des patients Covid-19 confirmés. Dix-sept (81 %) patients consituaient des cas sévère, définis cliniquement par :
– une fréquence respiratoire ≥ 30/min,
– une saturation pulsée en oxygène (SpO2) ≤ 93 %,
– un ratio pression artérielle en oxygène/fraction inspirée en oxygène (PaO2/FiO2) ≤ 300 mmHg.
Quatre patients (19 %) étaient des cas critiques, définis par l’admission en unité de soins intensifs (insuffisance respiratoire aiguë obligeant à la ventilation mécanique, état de choc, défaillance d’organe autre associée). Tous les patients ont initialement reçu une semaine d’un traitement standard, incluant lopinavir, méthylprednisone, oxygénothérapie et traitement symptomatique. Une cure de tocilizumab (400 mg IV une fois) leur a ensuite été administrée en raison de la décompensation secondaire de leur pathologie virale. IL s’en est suivi, dans un délai de cinq jours après cette cure, une nette amélioration de l’ensemble des paramètres :
– cliniques :
- disparition de la fièvre et des signes respiratoires de pneumonie,
- sevrage en oxygène ou en ventilation artificielle,
– biologiques : normalisation de la CRP, des lymphocytes et de l’hypoxémie,
– scanographiques : régression des opacités en verre dépoli témoignant de la réparation des dommages tissulaires pulmonaires.
Dix-neuf patients (90 %), dont deux initialement critiques, sont sortis de l’hôpital après une durée moyenne de séjour de 13,5 jours (± 3,1) après la cure de tocilizumab. Les deux autres patients sont restés hospitalisés mais se sont améliorés, sans dépendre des paramètres de ventilation invasive. Les auteurs de ce travail avaient formulé l’hypothèse d’un taux estimé de mortalité de 20 % pour les cas sévères de Covid-19 ; il n’y a eu aucun décès dans leur série. Ils concluent que le tocilizumab pourrait avoir un impact positif sur le risque accru de morbimortalité préalablement établi. Ils soulignent cependant plusieurs limites de leur étude : il s’agit d’une étude observationnelle rétrospective de petite taille qui n’a pas recruté de groupe contrôle ni analysé l’ajustement de facteurs confondants d’où l’émergence de biais statistiques de probabilité. À noter que l’étude n’a pas rapporté d’effets indésirables sur la totalité des 21 patients, sans qu’il y ait eu une aggravation de pathologies préexistantes.
En conclusion
Le tocilizumab pourrait être utilisé chez les patients atteints de formes graves de la Covid-19, éventuellement en association avec des traitements conventionnels, voire à des antiviraux. Puisqu’il s’opposerait aux effets du syndrome de libération des cytokines en bloquant le récepteur de l’IL-6, il faut considérer cette biothérapie comme une thérapeutique spécifique de la composante inflammatoire systémique aiguë de la pathologie virale. À ce jour, afin d’assurer la pertinence d’administration du produit, celle-ci devrait être davantage identifiée précocement à partir de la concordance d’un ensemble de paramètres associant la clinique, les biomarqueurs inflammatoires, le taux sérique des cytokines (l’IL-6) et la scanographie pulmonaire. Des recommandations thérapeutiques sont certainement à attendre à partir des résultats d’essais cliniques randomisés de bonne envergure.
Liens d’intérêt
L’auteur déclare n’avoir aucun lien d’intérêt en rapport avec cet article.
Références
1. Zhou Y, Fu B, Zheng X, et al. Pathogenic T cells and inflammatory monocytes incite inflammatory storm in severe Covid-19 patients. Natl Sci Rev, March 13, 2020. http://doi:10.1093/nsr/nwaa041
2. Covid-19: Consider cytokine storm syndromes and immunosuppression. Lancet 2020; 395: 1033-34.
3. Zhang C, Wu Z, Li J.-W, Zhao H, Wang G.-Q. The cytokine release syndrome (CRS) of severe Covid-19 and Interleukin-6 receptor (IL-6R) antagonist Tocilizumab may be the key to reduce the mortality. Int J Antimicrob Agents, April 5, 2020. https://doi.org/10.1016/j.ijantimicag.2020.105954
4. Zhang X, Song K, Tong F, et al. First case of Covid-19 in a patient with myeloma successfully treated with tocilizumab. Blood Adv 2020; 4(7): 1307-10.
5. Michot J.-M, Albiges L, Chaput N, et al. Tocilizumab, an anti-IL6 receptor antibody, to treat Covid-19-related respiratory failure : a case report. Ann Oncol, March 27, 2020. https://doi.org/10.1016/j.annonc.2020.03.300
6. Bennardo F, Buffone C, Giudice A. New therapeutic opportunities for Covid-19 patients with Tocilizumab : Possible correlation of interleukine-6 receptor inhibitors with osteonecrosis of the jaws. Oral Oncol, March 21, 2020. https://doi.org/10.1016/j.oraloncology.2020.104659
7. Xu X, Han M, Li T, et al. Effective treatment of severe Covid-19 patients with Tocilizumab. http://chinaxiv.org/abs/202003.00026
